本品为人血液制品,因原料来自人血,虽然对原料血浆进行了相关病原体的筛查,并在生产工艺中加入了去除和灭活病毒的措施,但理论上仍存在传播某些已知和未知病原体的潜在风险,临床使用时应权衡利弊。
>国内首家血液制品GMP认证企业
>国内首家采用双重病毒灭活工艺用于生产
>国内首家采用全自动采浆机和全自动洗瓶灭菌罐装生产线的生产企业
>血浆优质安全,多道ELISA(酶联免疫法)和核酸扩增技术检测
>不含防腐剂和抗生素,纯度高,稳定性好
>全面与世界接轨的标准化体系认证

请仔细阅读说明书并在医师指导下使用
本品为人血液制品,因原料来自人血,虽然对原料血浆进行了相关病原体的筛查,并在生产工艺中加入了去除和灭活病毒的措施,但理论上仍存在传播某些已知和未知病原体的潜在风险,临床使用时应权衡利弊。
[药品名称]
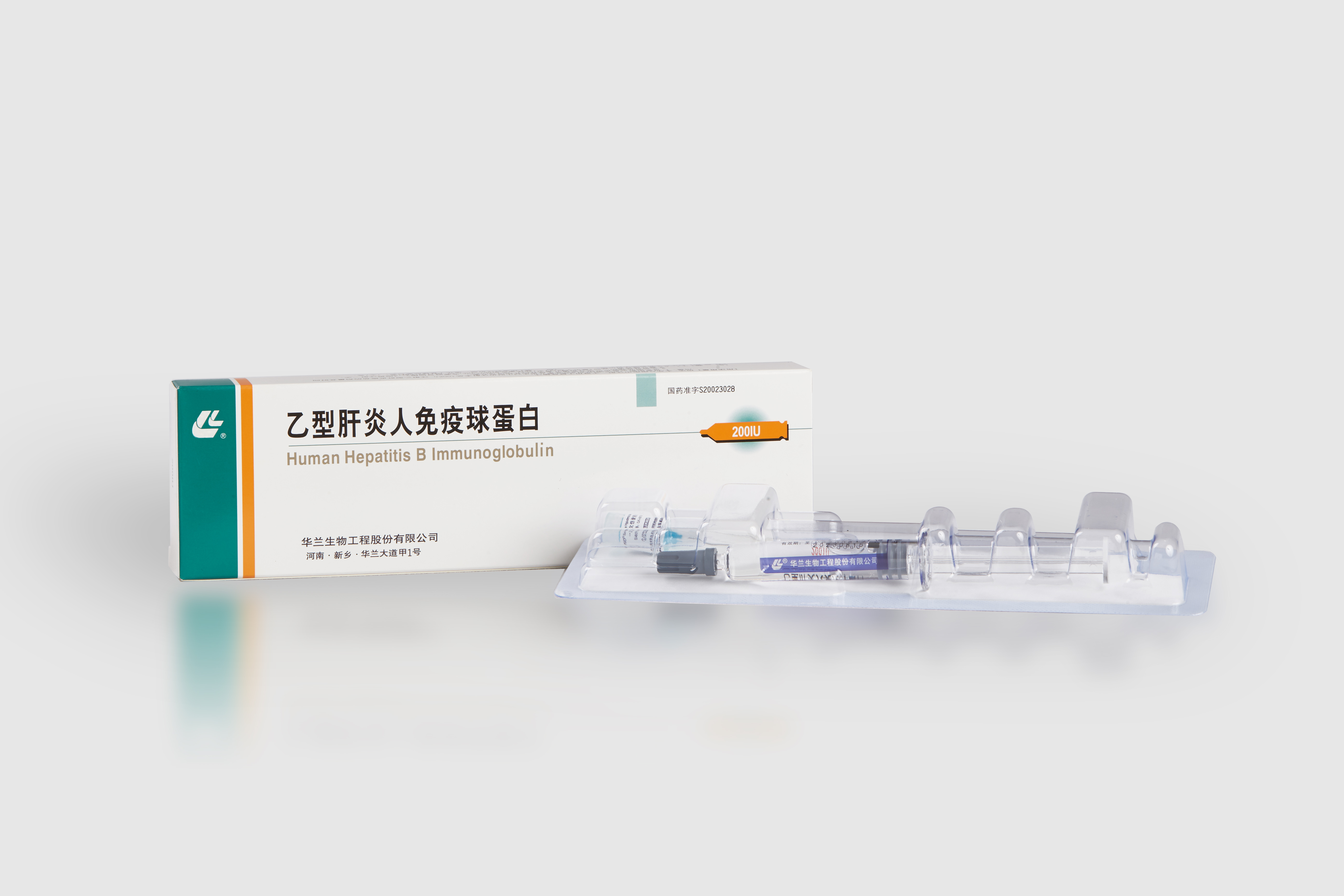
通用名称:乙型肝炎人免疫球蛋白
英文名称:Human Hepatitis B Immunoglobulin
汉语拼音:Yixing Ganyan Ren Mianyiqiudanbai
[成份]
本品活性成份为乙型肝炎人免疫球蛋白,辅料为葡萄糖、聚山梨酯80、氯化钠、甘氨酸、注射用水。
[性状]
本品应为无色或淡黄色澄明液体,可带乳光,不应出现浑浊。
[适应症]
主要用于乙型肝炎预防。
适用于:
1.乙型肝炎表面抗原( HBsAg )阳性的母亲所生的婴儿。
2.意外感染的人群。
3.与乙型肝炎患者和乙型肝炎病毒携带者密切接触者。
[规格]
200IU/支(2.0ml) 每支含抗-HBs效价200IU,装量2.0ml。
[用法用量]
用法:
本品只限肌内注射,不得用于静脉输注。
用量:
1.母婴阻断:HBsAg阳性母亲所生婴儿出生24小时内注射本品100IU;注射乙型肝炎疫苗的剂量及时间见乙型肝炎疫苗说明书或按医生推荐的其他适宜方案。
2.乙型肝炎预防:一次注射量儿童为100IU,成人为200IU,必要时可间隔3~4周再注射一次。
3. 意外感染者,立即(最迟不超过7天)按体重注射8IU~10IU/kg,隔月再注射1次。
[不良反应]
一般不会出现不良反应,少数人有红肿、疼痛感,无需特殊处理,可自行恢复。
[禁忌]
1.对人免疫球蛋白过敏或有其他严重过敏史者。
2.有IgA抗体的选择性IgA缺乏者。
[注意事项]
1.本品应为无色或淡黄色可带乳光澄明液体。久存可能出现微量沉淀,但一经摇动应立即消散,如有摇不散的沉淀或异物不得使用。
2.注射器破裂、过期失效者不得使用。
3.本品开启后,应一次输注完毕,不得分次使用或给第二个人使用。
[孕妇及哺乳期妇女用药]
未专门进行该项针对性试验研究,且无系统可靠的参考文献。
[儿童用药]
见用法用量项。
[老年用药]
未专门进行该项针对性试验研究,且无系统可靠的参考文献。
[药物相互作用]
凡对免疫球蛋白有相互作用的药物可能会对本品产生相互作用。
[药物过量]
可能产生变态反应和因剂量大在注射部位造成疼痛感。
[药理毒理]
本品含有高效价的抗乙型肝炎表面抗原抗体(抗-HBs),能与相应抗原专一结合起到被动免疫的作用。
[药代动力学]
未进行该项针对性实验研究,以下数据来自相关文献报道。
吸收:肌肉注射该品后,抗-HBs从注射部位缓慢释放到血液循环系统中,2至4天后达到最大浓度。
动力学:免疫球蛋白的半衰期大约为28天,IgG与病毒的复合物可以被网状内皮系统清除。
[贮藏]
于2~8°C避光保存和运输。
[包装]
预灌封注射器、溴化丁基橡胶塞包装。1支/盒。
[有效期]
自生产之日起36个月。
[执行标准]
《中华人民共和国药典》( 2020年版三部)
[批准文号]
国药准字S20023028
[上市许可持有人]
名称:华兰生物工程股份有限公司
注册地址:河南省新乡市华兰大道甲1号
[生产企业]
企业名称:华兰生物工程股份有限公司
生产地址:河南省新乡市华兰大道甲1号
邮政编码:453003
电话号码:(0373)3519992
传真号码:(0373)3519991
网址:http://www.hualanbio.com